首个靶向LAG-3分子的抗肿瘤免疫疗法问世
来源:源道隆医学科技 | 发布时间:2022-03-21 15:40:40 |
LAG-3是一个发现已有30年历史的免疫检查点蛋白。上世纪90年代,免疫学家从NK细胞系中克隆到它的基因并鉴定了表达的蛋白分子,给它取名为淋巴细胞激活基因3(LAG-3)。与PD-1和CTLA-4类似,LAG-3在幼稚T细胞(naïve T cells)表面并不表达。但随着抗原的刺激,它会在CD4和CD8阳性的T细胞上表达,而表达水平越高,其免疫抑制力也越强。HIV等慢性病毒感染的研究发现,抗原的长期刺激下特异性T细胞的衰竭与LAG-3长期持续表达相关。而与之相反的是,抑制LAG-3可以重塑耗竭T细胞的活力。这种调控机制与PD-1分子非常相似。因此,目前不少研究癌症免疫疗法的公司一直在关注这个免疫检查点分子。

与PD-1相比,LAG-3的生物学功能更加复杂。在T细胞表面LAG-3主要起抑制信号作用。当CD8阳性的T细胞表面的LAG-3结合了II类MHC分子时,如果T细胞受体还结合了抗原呈递细胞表面的I类MHC分子,那么LAG-3就会终止下游的钙信号,导致细胞因子生产的减少。这样的负反馈机制能在不需要免疫反应的时候很快将其关闭。但另一方面,LAG-3也能激活抗原呈递细胞。当抗原呈递细胞表面的II类MHC分子结合可溶性的LAG-3后,就会被激活。而这些抗原呈递细胞的激活,又会进一步激活细胞毒性的CD8阳性T细胞,激活免疫反应。
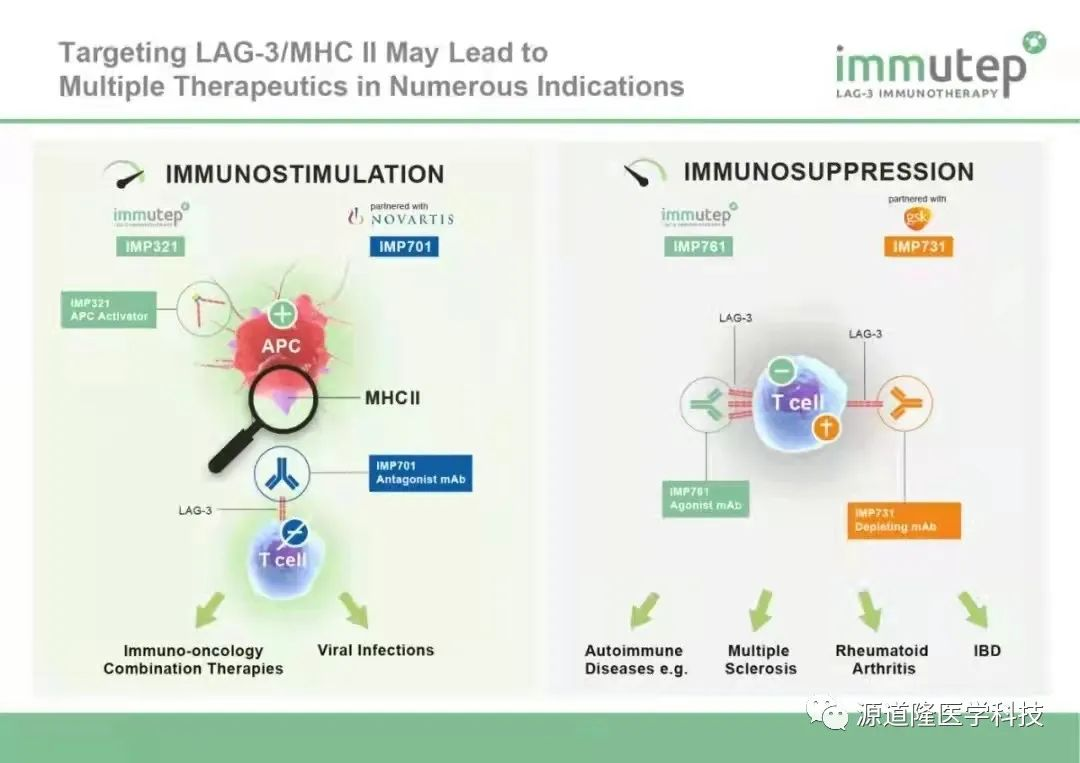
针对LAG-3的肿瘤免疫疗法研发过程并非一帆风顺。最早获得的LAG-3特异性抗体relatlimab是用来治疗恶性黑色素瘤的,然而,早期临床试验发现其单独疗法活性非常有限,几乎不能降低肿瘤体积。2017年,百时美施贵宝宣布relatlimab与抗PD-1疗法Opdivo的组合疗法在黑色素瘤中取得了一定的效果。研究表明,如果肿瘤周围的免疫细胞表达LAG-3的水平较高,组合疗法取得的客观缓解率就能达到18%。相反,如果周围的免疫细胞几乎不表达LAG-3,客观缓解率就只有5%。2021年,百时美施贵宝又在ASCO的摘要中公布了其2/3期临床试验的结果,表明relatlimab与Opdivo的组合疗法与Opdivo单药相比,在既往未经治疗的转移性或不可切除的黑色素瘤患者中,表现出具有统计学意义和临床意义的无进展生存期(PFS)获益。接受联合治疗的患者中位PFS显著延长,为10.12个月(95% CI: 6.37-15.74),而接受Opdivo单药的患者为4.63个月(95% CI: 3.38-5.62)。该公司的新闻稿也指出,这是在转移性黑色素瘤中,首个相对于抗PD-1抗体单药治疗还能具有统计学获益的治疗方案。
去年9月,百时美施贵宝宣布FDA已授予relatlimab和Opdivo组合疗法优先审评资格。昨天(3月19日),FDA批准relatlimab成为了首个问世的LAG-3抗体。对于PD-1和LAG-3的联合作用,医药评论专栏Endpoints的文章做了一个形象的比喻:不同的免疫检查点就像是T细胞表面的不同开关。如果肿瘤想要逃脱免疫系统的监控,必须关闭T细胞的开关。PD-1是其中比较主要的那个,而PD-1抑制剂能卡住这个开关,使其无法被关闭;在这个情况下,肿瘤为了生存,必须去找其它小开关,比如LAG-3。但因为不同肿瘤选择的小开关并不一致,所以针对LAG-3的抗体可能只会针对少数的肿瘤。源道隆医学观察将继续关注靶向LAG-3及其他免疫检查点的肿瘤抗体药物。

上一篇:
抗CD39抗体TTX-030在胃癌治疗中获得重大进展 下一篇:
IgM型抗体药物研发的新动态


